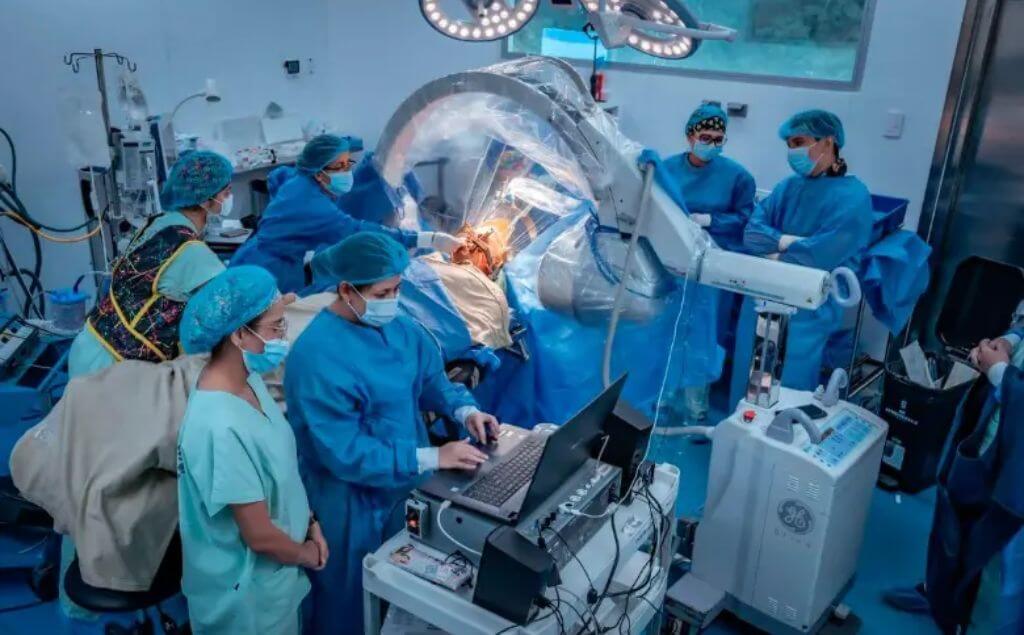



Un ensayo internacional confirma que fremanezumab reduce los días de migraña en niños y adolescentes, con un perfil de seguridad favorable.
Un ensayo clínico internacional con participación del Hospital Vall d’Hebron demostró que el fármaco fremanezumab reduce de forma significativa la frecuencia de la migraña en niños y adolescentes. El estudio, denominado SPACE y publicado en The New England Journal of Medicine, evaluó por primera vez este tratamiento preventivo en población pediátrica.
La migraña afecta al 11 % de los niños y adolescentes. Los episodios provocan dolor intenso, náuseas, vómitos y sensibilidad a la luz o al ruido. Estos síntomas alteran la asistencia escolar, el rendimiento académico y la vida social, además de generar un impacto emocional en las familias.
Otras noticias: Renuncias y reemplazos de alto perfil al tiempo que se extienden secuelas del caso Epstein
Hasta ahora, los médicos contaban con pocas opciones preventivas específicas para esta franja de edad. Muchos tratamientos carecían de evidencia sólida o no estaban diseñados para menores.
El estudio de fase 3 incluyó a más de 230 pacientes de entre 6 y 17 años con migraña episódica. Durante el ensayo, los participantes recibieron inyecciones subcutáneas de fremanezumab o placebo y registraron la frecuencia de los episodios.
Los resultados mostraron que el grupo tratado redujo en promedio cerca de 2,5 días de migraña al mes, frente a 1,4 días en el grupo placebo. Además, el 47 % de los pacientes que recibió el fármaco logró disminuir al menos un 50 % sus días de dolor, casi el doble que en el grupo de control.
Léase también: Cámara de Diputados argentina debate proyecto de Milei para bajar a 14 años edad de imputabilidad
Fremanezumab es un anticuerpo monoclonal que actúa sobre el péptido relacionado con el gen de la calcitonina (CGRP), una molécula implicada en los ataques de migraña. En adultos ya mostró eficacia y buen perfil de seguridad.
En población pediátrica, el ensayo confirmó efectos adversos leves y similares al placebo, principalmente reacciones locales en la zona de la inyección. El medicamento aún debe completar los procesos regulatorios antes de su aprobación específica para menores.
Te puede interesar: Gobierno colombiano busca atender inundaciones con nueva declaración de emergencia económica










.jpg)